Categorías
nuevo blog
- Guía de selección de electrolitos para baterías: lo que los gerentes de compras deben saber.
- Equipamiento para laboratorios de pilas de botón: La lista de verificación completa para laboratorios de I+D de baterías
- Comparación de materiales para cátodos de baterías: NMC vs LFP vs NCA
- Tendencias en la fabricación de baterías de iones de litio para 2026: Guía para compradores B2B
- Guía paso a paso del proceso de fabricación de baterías de iones de litio
Etiquetas
Electrolitos cerámicos Na3Zr2Si2PO12 para batería de iones de Na
Na3Zr2Si2PO12 Cerámica Electrolitos para baterías de iones de Na: preparación mediante el método de secado por aspersión y sus Propiedad
Autorï¼LI Wenkai, ZHAO Ning, BI Zhijie, GUO Xiangxin. Electrolitos cerámicos Na3Zr2Si2PO12 para baterías de iones de Na: preparación mediante Método de secado por aspersión y sus propiedades. Revista de materiales inorgánicos, 2022, 37 (2): 189-196 DOI:10.15541/jim20210486
Resumen
Baterías de iones de Na, que actualmente utilizan materiales orgánicos inflamables y explosivos. electrolitos, ahora es urgente desarrollar sólidos de iones de sodio de alto rendimiento electrolito para realizar una aplicación más segura y práctica. Na3Zr2Si2PO12 es uno de los electrolitos sólidos de sodio más prometedores por su amplia ventana electroquímica, alta resistencia mecánica, estabilidad superior del aire y alta conductividad iónica. Pero su mezcla no homogénea de las partículas cerámicas con los aglutinantes provoca Muchos más poros en los cuerpos verdes dificultan la obtención de alta densidad. y electrolitos cerámicos de alta conductividad después de la sinterización. En este caso, el spray Se utilizó un método de secado para permitir que las partículas de Na3Zr2Si2PO12 recubiertos uniformemente con aglutinantes y granulados en secundarios esféricos. El Las partículas distribuidas normalmente preparadas pueden entrar en contacto eficazmente entre sí y Reducir la porosidad del cuerpo verde cerámico. Después de la sinterización, cerámica Na3Zr2Si2PO12. Los gránulos a través del secado por aspersión muestran una densidad relativa del 97,5 %. y conductividad iónica de 6,96×10-4 Sâcm-1 en la habitación temperatura. Por el contrario, la densidad relativa y la temperatura ambiente Conductividad iónica de pellets cerámicos Na3Zr2Si2PO12 preparados sin secado por aspersión son sólo 88,1% y 4,94Ã10-4 Sâcm-1, respectivamente.
Palabras claveï¼ electrolito sólido; método de secado por aspersión; densidad; conductividad iónica; Na3Zr2Si2PO12
Los iones de sodio y los iones de litio pertenecen a el primer grupo principal, tienen propiedades químicas e intercalación similares y son ricos en reservas de recursos. Por lo tanto, las baterías de iones de sodio puede complementar las baterías de iones de litio [1, 2, 3]. Baterías de iones de sodio que contienen Los electrolitos orgánicos volátiles e inflamables presentan problemas de seguridad y son limitados. densidad de energía. Si se utilizan electrolitos sólidos en lugar de electrolitos líquidos, Se espera que los problemas de seguridad se resuelvan [4,5,6,7,8]. Electrolitos sólidos inorgánicos Tienen una amplia ventana electroquímica y pueden combinarse con cátodos de alto voltaje. materiales, aumentando así la densidad energética de las baterías [9]. Sin embargo, Los electrolitos sólidos enfrentan desafíos tales como baja conductividad iónica y dificultades. Transmisión de iones en la interfaz entre electrodos y electrolitos. Mientras Para optimizar la interfaz, primero es necesario encontrar electrolitos sólidos con alta conductividad iónica [10, 11, 12].
Actualmente, el ion sodio más estudiado Los electrolitos sólidos inorgánicos incluyen principalmente Na-βâ-Al2O3, tipo NASICON y sulfuro. Entre ellos, los de iones rápidos tipo NASICON (Sodium Super Ion Conductors). Los conductores tienen un gran potencial en aplicaciones de baterías de iones de sodio de estado sólido. debido a su amplia ventana electroquímica, alta resistencia mecánica, estabilidad al aire y alta conductividad iónica [13,14]. Fue informado originalmente por Goodenough y Hong et al. [15,16]. La fórmula general es Na1+xZr2SixP3-xO12 (0â¤xâ¤3), que es una solución sólida continua formada por NaZr2(PO4)3 y Na4Zr2(SiO4)3 y tiene un canal de transmisión de Na+ tridimensional abierto. Na1+xZr2SixP3-xO12 tiene dos estructuras: estructura rombo (R-3c) y monoclínica. estructura (C2/c, 1,8â¤xâ¤2,2). Cuando x=2, Na3Zr2Si2PO12 tiene el valor iónico más alto. conductividad. A 300 °C, la conductividad iónica de Na3Zr2Si2PO12 puede alcanzar 0,2 Sâcm-1, que está cerca de la conductividad iónica de Na-βâ-Al2O3 (0,1~ 0,3 Sâcm-1) [15]. El ion actual a temperatura ambiente conductividad de Na3Zr2Si2PO12 reportada en la literatura [17,18] es aproximadamente ~10-4 Sâcm-1. dopaje elemento Los métodos se utilizan comúnmente para mejorar la conductividad iónica. Desde el sólido NASICON El electrolito tiene una estructura de esqueleto abierto, puede doparse con una variedad de elementos. Por ejemplo, los elementos que reemplazan al Zr4+ incluyen Mg2+, Zn2+, Al3+, Sc3+, Y3+, La3+, Ti4+, Hf 4+, Nb5+, Ta5+, etc. [17, 18, 19, 20, 21, 22]. Aquellos que reemplazan a P5+ incluyen Ge5+ y As5+ [22]. Además del dopaje elemental, aumentar la densidad de las láminas cerámicas Na3Zr2Si2PO12 también es un método común para mejorar su conductividad iónica. Recientemente, Yang et al. [18] elemento usado dopaje combinado con sinterización en una atmósfera de oxígeno para sintetizar altamente Na3.2+2xZr2-x ZnxSi2.2P0.8O12 denso (0â¤xâ¤0.15). Cuando x=0.1, la habitación La conductividad iónica de temperatura alcanza el valor máximo (5,27Ã10-3 Sâcm-1). Los métodos de preparación del electrolito cerámico Na3Zr2Si2PO12. incluyen: sinterización convencional (CS), sinterización en fase líquida (LPS), chispa sinterización por plasma (SPS), sinterización por microondas (MWS) y proceso de sinterización en frío (CSP) [18-21,23-29]. Entre ellos, Huang et al. [20] utilizó sinterización convencional Métodos para aumentar la densidad de las cerámicas mediante dopaje con Ga3+. una ceramica Se obtuvo electrolito con mayor conductividad iónica a temperatura ambiente (1,06×10-3 Sâcm-1) y menor conductividad electrónica (6,17×10-8 Sâcm-1). ZHANG et al. [21] adoptó la sinterización convencional método introduciendo el catión La3+. Se forma la fase intermedia Na3La(PO4)2. en el límite de grano, y una lámina cerámica Na3.3Zr1.7La0.3Si2PO12 con un Se obtiene una densidad de hasta el 99,6%. El ion correspondiente a temperatura ambiente La conductividad puede alcanzar 3,4Ã10-3 Sâcm-1. WANG et al. [23] usado Sinterización por microondas (MWS) para obtener cerámicas Na3Zr2Si2PO12 de alta densidad. del 96% a una temperatura de sinterización baja de 850°C y se mantuvo solo durante 0,5 h, reduciendo la sinterización costos. Los valores de densidad relativa (relative), conductividad iónica (Ït) y Energía de activación (Ea) de electrolitos cerámicos preparados por diferentes métodos. se enumeran en la Tabla 1.
Tabla 1 Parámetros clave del tipo NASICON Materiales para diferentes métodos de sinterización
|
Método de sinterización |
Composición |
Sinterización |
Sinterización |
Tiempo/h |
relativo/% |
p/(Sâcm-1) |
Ea/eV |
Ref. |
|
CSP |
Na3.256Mg0.128Zr1.872Si2PO12 |
140 |
Ninguno |
1 |
82,9 |
0.41´10-4 |
- |
[19] |
|
FH-CSP |
Na3Zr2Si2PO12 |
375 |
NaOH |
3 |
93 |
2.2´10-4 |
0,32 |
[24] |
|
LPS |
Na3Zr2Si2PO12 |
1150 |
NaF |
24 |
- |
1.7´10-3 |
0,28 |
[25] |
|
LPS |
Na3Zr2Si2PO12 |
900 |
Na3BO3 |
10 |
93 |
1.4´10-3 |
- |
[26] |
|
LPS |
Na3Zr2Si2PO12 |
1175 |
Na3SiO3 |
10 |
93 |
1.45´10-3 |
- |
[27] |
|
SPS |
Na3.4Zr1.6Sc0.4Si2PO12 |
1100 |
KOHaq |
0,1 |
95 |
9.3´10-4 |
- |
[28] |
|
SPS |
Na3Zr2Si2PO12 |
1210 |
Ninguno |
0,5 |
97,0 |
1.7´10-3 |
0,28 |
[29] |
|
MWS |
Na3Zr2Si2PO12 |
850 |
Ninguno |
0,5 |
96 |
2.5´10-4 |
0,31 |
[23] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Ninguno |
16 |
71,4 |
1.7´10-4 |
0,36 |
[20] |
|
CS |
Na3.1Zr1.9Ga0.1Si2PO12 |
1250 |
Ninguno |
16 |
86,5 |
1.06´10-3 |
0,29 |
[20] |
|
CS |
Na3Zr2Si2PO12 |
1200 |
Ninguno |
24 |
87,6 |
6.7´10-4 |
0,353 |
[21] |
|
CS |
Na3.3Zr1.7La0.3Si2PO12 |
1200 |
Ninguno |
24 |
99,6 |
3.4´10-3 |
0,291 |
[21] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Ninguno |
- |
84.02 |
2.17´10-4 |
0,407 |
[18] |
|
O2-CS |
Na3.4Zr1.9Zn0.1Si2.2P0.8O12 |
1250 |
Ninguno |
- |
99,46 |
5.27´10-3 |
0,285 |
[18] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Ninguno |
6 |
88.1 |
4.94´10-4 |
0,34 |
Este trabajo |
|
SD-CS |
Na3Zr2Si2PO12 |
1250 |
Ninguno |
6 |
97,5 |
6.96´10-4 |
0,32 |
Este trabajo |
CS: sinterización convencional; SD: secado por aspersión; O2-CS: sinterización convencional en estado puro oxígeno; CSP: proceso de sinterización en frío; FH-CSP: sinterización en frío con hidróxido fundido proceso; MWS: sinterización por microondas; LPS: sinterización en fase líquida; SPS: chispa sinterización por plasma
Los métodos convencionales utilizan polvo preparado por sinterización directa para mezclar con un aglutinante para producir polvo de cuerpo cerámico, y luego someterse a moldeado en polvo y sinterización a alta temperatura para obtener cerámica [30, 31, 32]. Sin embargo, durante el proceso de molienda y mezclado, debido a una mezcla desigual del aglutinante y las partículas cerámicas y el mal contacto entre las partículas, hay Hay muchos poros dentro del cuerpo verde, lo que dificulta la preparación de la cerámica. Electrolitos de alta densidad y alta conductividad iónica. El secado por aspersión es un Método de secado rápido que utiliza un atomizador para dispersar la suspensión en gotas. y utiliza aire caliente para secar las gotas para obtener polvo. Las partículas de la El polvo preparado mediante secado por aspersión es esférico y el aglutinante se puede distribuir uniformemente. recubierto en la superficie de las partículas [33]. KOU et al. [34] secado por aspersión usado combinado con sinterización a alta temperatura para sintetizar electrolito sólido Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 (LATSP) con iónico a alta temperatura ambiente conductividad. Cuando x = 0,05, la conductividad iónica a temperatura ambiente alcanza un máximo de 1.053Ã10-4 Sâcm-1, y el compactado La densidad es de 2,892 gâcm-3, que está cerca de la densidad teórica. de LATSP de 2,94 gâcm-3. Se puede observar que el secado por aspersión tiene ciertas ventajas en la mejora de la densidad y la conductividad iónica de la cerámica electrolitos. En vista de las ventajas del secado por aspersión, el efecto del elemento Se debe considerar el dopaje sobre la densidad cerámica y la conductividad iónica. Este El estudio seleccionó Na3Zr2Si2PO12 como objeto de investigación e introdujo el aerosol. método de granulación en la preparación preliminar de materiales en polvo para Prepare electrolito cerámico Na3Zr2Si2PO12 con alta densidad y alto contenido iónico. conductividad.
1 Método experimental
1.1 Preparación del material
Método de preparación del polvo Na3Zr2Si2PO12: Pesar Na2CO3 (Aladdin, 99,99%), NH4H2PO4 (Aladdin, 99%), ZrO2 (Aladdin, 99,99%), y SiO2 (Aladdin, 99,99%) según la relación estequiométrica. En para compensar la volatilización de Na y P durante la sinterización proceso, la materia prima contiene un exceso de 8% Na2CO3 y un 15% de exceso de NH4H2PO4 [25]. Se utilizaron bolas de circonio como medio de molienda de bolas, el La relación de peso de material/bola fue de 1:3, se usó etanol absoluto como dispersión. medio, y se utilizó el molino de bolas para la molienda de bolas durante 12 h. El molido de bolas La suspensión se secó en una estufa a 80 °C durante 12 h. El polvo seco se molió y Se pasó a través de un tamiz de malla 150 (100 μm) y luego se transfirió a una temperatura de 400 °C. crisol de alúmina durante 2 h. Eliminar CO32- y NH4+ del precursor, luego calentar hasta 1000~1150°C para la calcinación, y recocerlo después de 12 horas para obtener Na3Zr2Si2PO12 en polvo.
Método de preparación de cerámica Na3Zr2Si2PO12. hojas: Para explorar el efecto del tamaño de partícula de Na3Zr2Si2PO12 en la densidad de láminas cerámicas, se diseñaron dos conjuntos de experimentos de control. El El primer grupo utilizó métodos convencionales, añadiendo 2% (fracción en masa) de polivinilo. aglutinante de alcohol (Aladdin, Mw~205000) al polvo de fase pura Na3Zr2Si2PO12, añadiendo etanol absoluto y molienda de bolas durante 12 h. El polvo después de la molienda de bolas es secado, triturado y tamizado para obtener un polvo recubierto con un aglutinante sobre la partícula superficie. El polvo se prensa uniaxialmente en frío a 200 MPa utilizando un acero inoxidable. molde de acero para hacer un cuerpo verde de Ï12 mm, registrado como GB. . Para reducir la volatilización de Na y P durante el proceso de sinterización de láminas cerámicas, El cuerpo verde fue enterrado en el polvo madre y sinterizado a 1250°C durante 6 horas y luego recocido a una velocidad de calentamiento de 4°C/min. El obtenido El electrolito cerámico Na3Zr2Si2PO12 fue designado CS-NZSP. El segundo grupo utilizó un secador por pulverización (ADL311S, Yamato, Japón) para granular el polvo de Na3Zr2Si2PO12. Agregue 2% (fracción de masa) de aglutinante de alcohol polivinílico (Aladdin, Mw ~205000) y 2% dispersante de polietilenglicol (Aladdin, Mn=1000) al polvo de Na3Zr2Si2PO12, y añadir etanol absoluto. Preparar una suspensión con un contenido sólido del 15% en masa. fracción y molino de bolas durante 12 h. La suspensión molida con bolas se secó por aspersión. con una temperatura de entrada de 130°C y un caudal de alimentación de 5 ml/min. El El polvo de Na3Zr2Si2PO12 se recogió a través de un separador ciclónico. la tableta y los procesos de sinterización cerámica fueron los mismos que los del primer grupo, y El cuerpo verde Na3Zr2Si2PO12 obtenido y el electrolito cerámico se registraron como SD-GB y SD-CS-NZSP respectivamente. Tratamiento de pulido superficial de cerámica. baldosas: Primero use papel de lija de malla 400 (38 μm) para un pulido rugoso y luego Utilice papel de lija de malla 1200 (2,1 μm) para un pulido fino hasta que la cerámica la superficie es lisa. Los diámetros del electrolito cerámico CS-NZSP y SD-CS-NZSP. Las láminas son (11,3 ± 0,1) y (10,3 ± 0,1) mm respectivamente, y el espesor es (1,0 ± 0,1) mm.
1.2 Caracterización física de los materiales
El análisis de fase de las muestras fue realizado utilizando un difractómetro de rayos X (XRD, Bruker, D8 Advance). El la fuente de radiación es CuKα, la presión del tubo es de 40 kV, el flujo del tubo es de 40 mA, la velocidad de escaneo es 2 (°)/min y el rango de escaneo es 2θ= 10°~80°. Exploración microscopio electrónico (SEM, Hitachi, S-4800) y microscopio electrónico de transmisión (TEM, JEOL, JEM-2100F) se utilizaron para analizar la morfología de las muestras, y el accesorio EDX configurado se utilizó para el análisis elemental.
1.3 Medición de la conductividad eléctrica de láminas cerámicas
La espectroscopia de impedancia electroquímica (EIS) de la muestra se probó utilizando una estación de trabajo electroquímica. la prueba El rango de frecuencia es de 7 MHz ~ 0,1 Hz, el voltaje aplicado es de 10 mV, la curva de prueba se coloca y se calcula la conductividad iónica de la pieza cerámica utilizando fórmula (1).
Ï=L/(RÃS) (1)
En la fórmula, L es el espesor de la lámina de cerámica (cm), R es la resistencia (Ω), S es el área del electrodo de bloqueo (cm2), y Ï es la conductividad iónica (Sâcm-1).
La conductividad electrónica de la muestra. Se probó utilizando polarización de corriente continua (CC), con un voltaje constante de 5 V y una duración de 5000 s. El valor de ordenadas después de la curva se vuelve estable. es el valor de la corriente de polarización. Utilice las fórmulas (2, 3) para calcular el Conductividad electrónica y número de migración de iones de sodio de la lámina cerámica.
Ïe=LÃI/(VÃS) (2)
t=(Ï-Ïe)/Ï (3)
En la fórmula, L es el espesor de la lámina de cerámica (cm), I es la corriente de polarización (A), V es el voltaje (V), S es el área del electrodo de bloqueo (cm2) y Ïe es la conductividad electrónica (Sâcm-1). Este trabajo utiliza Au como electrodo de bloqueo. Preparación de electrodo de bloqueo: utilice equipo de recubrimiento por evaporación con resistencia al alto vacío (VZZ-300) para evaporar la fuente de evaporación Au mediante calentamiento por resistencia, y evaporarlo sobre la superficie de la lámina cerámica. La lámina cerámica es fijado en una férula con un diámetro interior de 8 mm.
2 Resultados y discusión
2.1 Estructura y morfología de fases caracterización de Na3Zr2Si2PO12
Para optimizar la sinterización temperatura de Na3Zr2Si2PO12, el polvo se sinterizó a 1000, 1050, 1100 y 1150 ℃ respectivamente. Los patrones de difracción de rayos X de las muestras obtenidas. La sinterización a diferentes temperaturas se muestra en la Figura 1. Se puede ver De la figura que cuando la temperatura de sinterización es de 1000 ° C, la fase principal Se ha generado Na3Zr2Si2PO12, pero hay impurezas de Na2ZrSi2O7 y ZrO2. fases, y la intensidad del pico de difracción de la fase principal es débil y la El ancho del medio pico es ancho, lo que indica que el producto de sinterización tiene mala calidad. cristalinidad. Cuando la temperatura de sinterización es de 1100 ℃, la impureza ZrO2 La fase desaparece y la intensidad del pico de difracción de la impureza Na2ZrSi2O7 La fase se debilita, lo que indica que aumentar la temperatura de sinterización es beneficioso para eliminar la fase de impureza. Los picos de difracción de la Los productos sinterizados a 1100 y 1150 °C tienen anchos de medio pico más pequeños que los picos de difracción de los productos sinterizados a 1000 °C, lo que indica que la Cuanto mayor sea la temperatura de sinterización, mejor será la cristalinidad del producto. En comparación con el producto sinterizado de 1000 °C, los picos de difracción del producto sinterizado de 1150 °C El producto sinterizado se divide en 2θ = 19,2°, 27,5° y 30,5°. Esto demuestra que el El material cambia de una fase rómbica con baja conductividad iónica a una fase monoclínica con alta conductividad iónica [25,35]. Y el pico de difracción es consistente con el pico de difracción estándar PDF 84-1200, lo que indica que 1150°C es la temperatura de formación de fase del electrolito sólido Na3Zr2Si2PO12 con una estructura monoclínica de alta conductividad iónica.
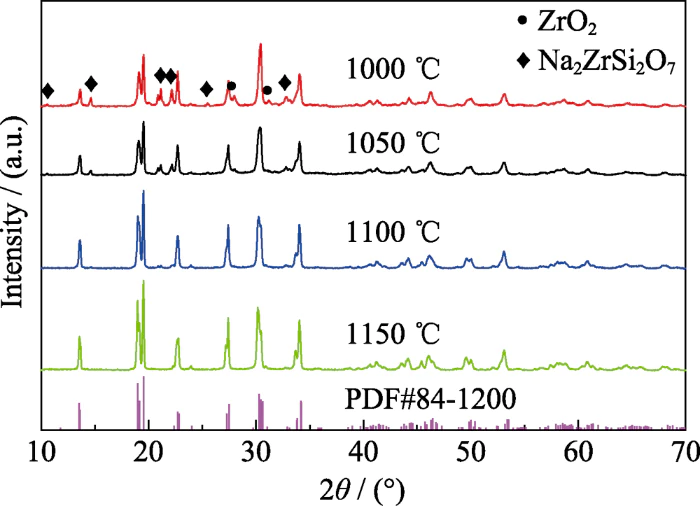
Fig. 1 DRX patrones de Na3Zr2Si2PO12 polvo sinterizado a diferentes temperaturas
La Figura 2 muestra fotografías SEM y fotografías TEM de Partículas de Na3Zr2Si2PO12 obtenidas mediante mezcla convencional y secado por aspersión. métodos. La Figura 2(a) es una fotografía SEM de partículas de Na3Zr2Si2PO12 después mezcla convencional. Se puede ver en la imagen que la forma del las partículas son irregulares y el diámetro de algunas partículas alcanza los 20 μm, indicando que las partículas después de la mezcla convencional son de gran tamaño y de forma desigual. La Figura 2 (b ~ c) muestra fotografías SEM de partículas de Na3Zr2Si2PO12. después del secado por aspersión. Las partículas son esféricas y el diámetro de las mismas es menos de 5 μm, lo que indica que la forma de la partícula es regular y la partícula La distribución del tamaño es más concentrada después del secado por aspersión. La figura 2 (d) es un TEM Foto de la superficie de partículas de Na3Zr2Si2PO12 después del secado por aspersión. El La superficie de la partícula está recubierta uniformemente con una capa de aglutinante con un espesor de aproximadamente 5 nm, lo que favorece un contacto más estrecho entre las partículas cerámicas.

Fig. 2 Imágenes SEM de partículas de Na3Zr2Si2PO12 después de la convencional mezcla (a) y secado por aspersión (b-c), e imagen TEM (d) de la superficie de la partícula de Na3Zr2Si2PO12 después de la aspersión secado
La figura 3 muestra el tamaño de partícula. diagrama de distribución del Na3Zr2Si2PO12 recubierto con alcohol polivinílico (NZSP) obtenido mediante mezcla convencional y el Na3Zr2Si2PO12 recubierto de alcohol polivinílico (SD-NZSP) obtenido por el método de secado por aspersión. Se puede observar que el El ancho del medio pico de la curva de distribución del tamaño de partículas SD-NZSP es más estrecho. que la de la curva de tamaño de partícula NZSP, lo que indica que el tamaño de partícula la distribución después del secado por aspersión es más concentrada. Esto es básicamente consistente con los resultados mostrados en las fotografías SEM en la Figura 2 (a, b). En Además, la curva de distribución del tamaño de partículas después del secado por aspersión está cerca de una distribución normal. Esta gradación del tamaño de partículas puede aumentar efectivamente la contacto entre partículas y reducir la porosidad del cuerpo verde. Como se muestra en la Tabla 2, la densidad del cuerpo verde Na3Zr2Si2PO12 preparado por el método de mezcla convencional es 83,01%, y la densidad del Na3Zr2Si2PO12 El cuerpo verde preparado mediante el método de secado por aspersión se incrementa al 89,12%. En orden explorar más a fondo el efecto del tamaño de partícula de Na3Zr2Si2PO12 sobre la densidad cerámica y conductividad, escaneo transversal, medición de densidad y Las pruebas de conductividad se realizaron en láminas cerámicas Na3Zr2Si2PO12 obtenidas por Métodos convencionales de mezcla y secado por aspersión.

Fig. 3 Na3Zr2Si2PO12 tamaño de partícula perfiles de mezcla convencional (NZSP) y secado por pulverización (SD-NZSP) medidos mediante analizador de partículas láser
Tabla 2 Parámetros de sinterización y parámetros de medición de densidad y resultados de medición del electrolito sólido Na3Zr2Si2PO12 cuerpos verdes y lámina cerámica
|
Muestra |
Temperatura de proceso/â |
Tiempo/h |
m/g |
retanol/(g·cm-3) |
msumergido/g |
rreal/(g·cm-3) |
teórico/(g·cm-3) |
relativo/% |
|
ES |
- |
- |
0,2902 |
0,785 |
0,2056 |
2.693 |
3.244 |
83.01 |
|
SD-GB |
- |
- |
0,2880 |
0.785 |
0,2098 |
2.891 |
3.244 |
89.12 |
|
CS-NZSP |
1250 |
6 |
0,2672 |
0,785 |
0,1938 |
2.858 |
3.244 |
88,10 |
|
SD-CS-NZSP |
1250 |
6 |
0,2644 |
0,785 |
0,1988 |
3.164 |
3.244 |
97,53 |
La figura 4 muestra la imagen física del Lámina cerámica Na3Zr2Si2PO12, su morfología transversal y elemental. diagrama de análisis. La Figura 4 (a) muestra la morfología de la sección transversal del Pieza cerámica obtenida por el método de sinterización convencional. fue observado que había muchos poros irregulares en la sección transversal de la lámina cerámica, y el diámetro de los poros locales superó los 5 μm. La razón es que el tamaño de las partículas después de la molienda es desigual, hay partículas más grandes y no hay cierre Contacto entre las partículas, lo que resulta en poros más irregulares en la cerámica. hoja durante el proceso de sinterización secundaria. La figura 4(b) muestra la Morfología transversal de la pieza cerámica obtenida mediante secado por aspersión. método. Los granos de cristal están en estrecho contacto entre sí y hay sin poros obvios. Esto muestra que las partículas de Na3Zr2Si2PO12 con forma regular Y la distribución concentrada del tamaño de partículas puede obtener fácilmente alta densidad. láminas cerámicas durante el proceso de sinterización secundaria. El aumento de la densidad también se refleja en el aumento de la contracción del cuerpo cerámico después sinterización, como se muestra en la Figura 4 (c). A la izquierda una pieza cerámica obtenida por el método de sinterización convencional, con un diámetro de 11,34 mm, y una contracción tasa de sólo el 5,5%; a la derecha una pieza cerámica obtenida por secado por aspersión método, con un diámetro de 10,36 mm y una tasa de contracción del 13,7%. Con el fin de explorar la composición de cada elemento en la muestra, se realizó un análisis elemental realizado en la sección transversal de la pieza cerámica (Figura 4(b)), y Figura Se obtuvo 4(d~g). El contenido de cada elemento se muestra en la Tabla 3. Cada elemento se distribuye uniformemente en la sección transversal de la pieza cerámica, y no hay agregación de elementos. Según la Tabla 3, se encuentra que la El porcentaje atómico de Na y P es 2,98:1, lo que es básicamente consistente con la fórmula química estándar de Na:P=3:1, lo que indica que el exceso de Na y P en el Las materias primas pueden compensar la volatilización de Na y P durante la proceso de sinterización.

Fig. 4 Imágenes SEM de secciones de corte para CS-NZSP (a) y SD-CS-NZSP (b), fotografías correspondientes (c) e imágenes de mapeo elemental (dg) de SD-CS-NZSP
Tabla 3 Análisis elemental de la sección de corte cerámico Na3Zr2Si2PO12 por pulverización secado/%
|
Elemento |
OK |
Na K |
Si K |
PK |
Zr L |
|
Porcentaje atómico |
60,10 |
15.09 |
9,94 |
5.06 |
9,81 |
|
Porcentaje de peso |
36,43 |
13.13 |
10.59 |
5,94 |
33,91 |
2.2 Densidad de láminas cerámicas Na3Zr2Si2PO12
El experimento midió la densidad de Láminas cerámicas Na3Zr2Si2PO12 mediante el método de Arquímedes [30]. Para poder estudiar el efecto del método de granulación sobre la densidad de la cerámica Na3Zr2Si2PO12 láminas, en los parámetros experimentales de preparación de láminas cerámicas, el parámetros experimentales (temperatura de sinterización, tiempo de mantenimiento, etc.) del El grupo experimental de control, excepto el método de granulación, se mantuvo igual. En para reducir el impacto de los errores de medición experimentales en la densidad resultados, las mediciones de densidad se repitieron en las muestras de láminas cerámicas obtenidos por cada método de preparación en el experimento. De lo experimental datos que se muestran en la Tabla 4, se puede ver que la densidad de la cerámica CS-NZSP láminas obtenidas por el método de sinterización convencional es del 88,1%, que es básicamente consistente con los resultados informados en la literatura [21]. la densidad de Las láminas cerámicas SD-CS-NZSP obtenidas mediante secado por aspersión pueden alcanzar el 97,5%, que es el valor más alto alcanzado actualmente por los métodos de sinterización convencionales sin elemento de dopaje. Es incluso mayor que la densidad de la cerámica Na3Zr2Si2PO12. láminas obtenidas por otros métodos de sinterización reportados en la literatura. Como método de sinterización por microondas (96%) [23], método de sinterización en frío (93%) [24], líquido método de sinterización en fase (93%) [26] y método de sinterización por plasma de descarga (97,0%) [29].
Tabla 4 Conductividad iónica de CS-NZSP y SD-CS-NZSP a temperatura ambiente
|
Muestra |
sb/(S·cm-1) |
sgb/(S·cm-1) |
st/(S·cm-1) |
Ea/eV |
|
CS-NZSP |
1.28Ã10-3 |
8.03Ã10-4 |
4.94Ã10-4 |
0,34 |
|
SD-CS-NZSP |
1.64Ã10-3 |
1.21Ã10-3 |
6.96Ã10-4 |
0,32 |
2.3 Rendimiento eléctrico Na3Zr2Si2PO12 prueba
La figura 5 (a) muestra la temperatura ambiente. espectro de impedancia electroquímica (EIS) de la oblea cerámica obtenida por método de sinterización convencional y método de secado por aspersión. El semicírculo en el La figura refleja las características de impedancia paralela del límite de grano. Impedancia y reactancia capacitiva. La intersección entre el lado izquierdo de el semicírculo y la abscisa representan la resistencia de la fibra. El La amplitud del semicírculo en la abscisa refleja la resistencia de la fibra. límite, y la línea oblicua después del semicírculo refleja la impedancia características de la interfaz electrodo de bloqueo/electrolito [36]. Por Ajustando el EIS en la Figura 4, la conductividad iónica de CS-NZSP y SD-CS-NZSP se puede obtener. Los datos experimentales se muestran en la Tabla 4. La habitación conductividad iónica de temperatura de SD-CS-NZSP obtenida por secado por aspersión método es 6.96Ã10-4 Sâcm-1, que es más alto que el de CS-NZSP (4.94Ã10-4 Sâcm-1) obtenido por el método de sinterización convencional. A través del análisis de datos del ajuste EIS, se puede ver que SD-CS-NZSP con mayor La densidad tiene una resistencia límite de grano más pequeña y una temperatura ambiente más alta iónica. conductividad.
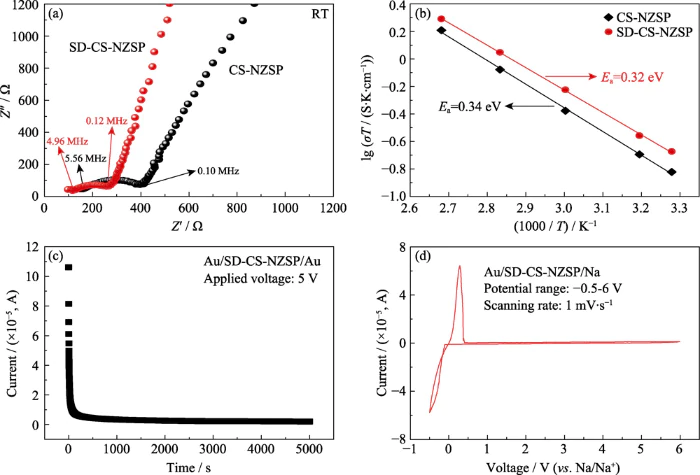
Fig. 5 (a) espectros EIS a temperatura ambiente y (b) Gráficos de Arrhenius de CS-NZSP y SD-CS-NZSP; (c) Polarización potenciostática de CC corriente y (d) ventana electroquímica para SD-CS-NZSP
La Figura 5(b) muestra las curvas de Arrhenius de temperatura ambiente a 100°C para láminas cerámicas obtenidas por diferentes preparaciones métodos. Se puede ver en la figura que sus conductividades aumentan con temperatura creciente. Cuando la temperatura alcanza los 100 °C, la conductividad de SD-CS-NZSP puede alcanzar 5.24Ã10-3 Sâcm-1, que es un orden de magnitud mayor que la conductividad a temperatura ambiente. Su energía de activación se ajusta según la ecuación de ArrheniusÏ=Aexp(-Ea/kT)[7]. Las energías de activación de Se obtuvo que CS-NZSP y SD-CS-NZSP eran 0,34 y 0,32 eV respectivamente, lo que son similares al informe de YANG et al. [18].
Los materiales de electrolitos sólidos deben tener tanto de alta conductividad iónica como de baja conductividad electrónica. Por lo tanto, el La conductividad electrónica de SD-CS-NZSP se midió mediante corriente continua. polarización (DC), y la curva de polarización correspondiente se muestra en la Figura 5c). Se puede ver en la figura que a medida que se prolonga el tiempo de prueba, el la corriente de polarización disminuye gradualmente; cuando el tiempo de prueba alcanza los 5000 s, la corriente de polarización (I=3,1 μA) ya no cambia a medida que transcurre el tiempo de prueba. prolonga. Calculada mediante las fórmulas (2, 3), la conductividad electrónica de SD-CS-NZSP es 1,23Ã10-7 Sâcm-1, y el ion sodio El número de migración es 0,9998. El estudio también midió la ventana electroquímica. de SD-CS-NZSP mediante voltamperometría cíclica (CV) [18]. Como se muestra en la Figura 5(d), dos Los picos de oxidación y reducción aparecen alrededor de 0 V, lo que representa la extracción. y deposición de sodio respectivamente [20]. Aparte de esto, ningún otro redox Se observaron picos dentro del rango de voltaje escaneado. Esto significa que hay No hay cambios en la corriente debido a la descomposición del electrolito en el voltaje. rango de 0 ~ 6 V, lo que indica que SD-CS-NZSP tiene buena estabilidad electroquímica. La amplia ventana electroquímica (6 V (frente a Na/Na+)) puede igualar el ion sodio. electrolito sólido hasta materiales catódicos de alto voltaje, como Materiales catódicos a base de níquel-manganeso, lo que es beneficioso para mejorar la Densidad de energía de las baterías de iones de sodio.
3 Conclusión
Se utilizó un método en fase sólida a alta temperatura. Se utiliza para sintetizar polvo de Na3Zr2Si2PO12 en fase pura a una temperatura de sinterización. de 1150°C introduciendo exceso de Na y P en el precursor. Usando secado por aspersión Para granular esféricamente el polvo, el aglutinante de alcohol polivinílico se aplica uniformemente. recubierto en la superficie de las partículas Na3Zr2Si2PO12 y el tamaño de partícula la distribución es cercana a la distribución normal. La densidad del preparado. La cerámica Na3Zr2Si2PO12 alcanza el 97,5%. Una mayor densidad puede reducir eficazmente Resistencia al límite de grano y la conductividad iónica alcanza 6,96 × 10-4 Sâcm-1 a temperatura ambiente, que es más alta que las láminas de cerámica. preparado por métodos de sinterización convencionales (4.94Ã10-4 Sâcm-1). Además, el Las cerámicas producidas por el método de secado por aspersión tienen una amplia ventana electroquímica. (6 V (frente a Na/Na+)) y se puede combinar con materiales catódicos de alto voltaje para aumentar la densidad de energía de la batería. Se puede observar que el spray El método de secado es un método eficaz para preparar electrolitos cerámicos Na3Zr2Si2PO12. con alta densidad y alta conductividad iónica, y es adecuado para otros tipos de electrolitos sólidos cerámicos.
Referencias
[1] JIAN Z L, ZHAO L, PAN H L, et al. Na3V2(PO4)3 recubierto de carbono como nuevo material de electrodo para baterías de iones de sodio. Comunicaciones de electroquímica, 2012,14(1):86-89.
[2] ZHAO L, ZHAO JM, HU Y S, et al. Tereftalato disódico (Na2C8H4O4) como material anódico de alto rendimiento para Batería de iones de sodio de bajo costo a temperatura ambiente. Materiales energéticos avanzados, 2012,2(8):962-965.
[3] RUAN Y L, GUO F, LIU J J, et al. Optimización del electrolito cerámico Na3Zr2Si2PO12 y la interfaz para alta Batería de sodio de estado sólido de alto rendimiento. Cerámica Internacional, 2019,45(2):1770-1776.
[4] VETTER J, NOVAK P, WAGNER MR, et al. Mecanismos de envejecimiento en baterías de iones de litio. Revista de fuentes de energía, 2005,147(1/2):269-281.
[5] KAMAYA N, HOMMA K, YAMAKAWA Y, et al. A Conductor superiónico de litio. Materiales naturales, 2011,10(9):682-686.
[6] TARASCON J M, ARMAND M. Cuestiones y Desafíos que enfrentan las baterías de litio recargables. Naturaleza, 2001,414(6861):359-367.
[7] KHOKHAR W A, ZHAO N, HUANG W L, et al. Diferentes comportamientos de penetración de metales en electrolitos sólidos de Na y Li. SCA Interfaces y materiales aplicados, 12(48):53781-53787.
[8] OUDENHOVEN J F M, BAGGETTO L, NOTTEN P H L. Microbaterías de iones de litio de estado sólido: una revisión de varios tres conceptos dimensionales. Materiales energéticos avanzados, 2011,1(1):10-33.
[9] ZHAO C L, LIU L L, QI X G, et al. Baterías de sodio de estado sólido. Materiales energéticos avanzados, 2017,8(17):1703012.
[10] HAYASHI A, NOI K, SAKUDA A, et al. Electrolitos vitrocerámicos superiónicos para sodio recargable a temperatura ambiente baterías. Comunicaciones de la naturaleza, 2012,3:856.
[11] LOU S F, ZHANG F, FU C K, et al. Problemas y desafíos de interfaz en baterías totalmente de estado sólido: litio, sodio, y más allá. Materiales avanzados, 2020,33(6):2000721.
[12] HUANG W L, ZHAO N, BIZ J, et al. Poder ¿Encontramos una solución para eliminar la penetración de Li a través de electrolitos sólidos de granate? Materiales hoy Nano, 2020,10:100075.
[13] JIAN Z L, HU Y S, JI X L, et al. Materiales estructurados NASICON para almacenamiento de energía. materiales avanzados, 2016,29(20):1601925.
[14] HOU W R, GUO X W, SHEN X Y, et al. Electrolitos sólidos e interfaces en baterías de sodio totalmente sólidas: avances y perspectiva. Nano Energía, 2018, 52:279-291.
[15] BUEN J B, HONG H Y P, KAFALAS J A. Transporte rápido de iones Na+ en estructuras esqueléticas. Boletín de investigación de materiales, 1976,11(2):203-220.
[16] HONG H Y P. Estructuras cristalinas y química cristalina en el sistema Na1+xZr2SixP3-xO12. Investigación de materiales Boletín, 1976,11(2):173-182.
[17] RAN LB, BAKTASH A, LI M, et al. Carolina del Sur, El co-dopaje NASICON aumenta el rendimiento de las baterías de iones de sodio de estado sólido. Materiales de almacenamiento de energía, 2021,40:282-291.
[18] YANG J, LIU G Z, AVDEEV M, et al. Baterías recargables de sodio ultraestables y de estado sólido. Cartas de Energía ACS, 2020,5(9):2835-2841.
[19] LENG H Y, HUANG JJ, NIE J Y, et al. Sinterización en frío y conductividades iónicas del sólido Na3.256Mg0.128Zr1.872Si2PO12 electrolitos. Revista de fuentes de energía, 2018,391:170-179.
[20] HUANG C C, YANG G M, YU WH, et al. Electrolitos sólidos Nasicon Na3Zr2Si2PO12 sustituidos con galio. Revista de aleaciones Y compuestos, 2021,855:157501.
[21] ZHANG Z Z, ZHANG Q H, SHI J N, et al. Un electrolito compuesto autoformable para baterías de sodio de estado sólido con ciclo de vida ultralargo. Materiales energéticos avanzados, 2017,7(4):1601196.
[22] ANANTHARAMULU N, RAO K K, RAMBABU G, et al. Una amplia revisión sobre materiales tipo Nasicon. Diario de materiales Ciencia, 2011,46(9):2821-2837.
[23] WANG X X, LIU Z H, TANG Y H, et al. Sinterización rápida y a baja temperatura por microondas de sólido Na3Zr2Si2PO12 Electrolitos para baterías de iones de Na. Revista de fuentes de energía, 2021,481:228924.
[24] GRADY Z M, TSUJI K, NDAYISHIMIYE A, et Alabama. Densificación de un electrolito de iones de sodio NASICON en estado sólido por debajo de 400 °C mediante sinterización en frío con un disolvente de hidróxido fundido. Materiales de energía aplicada ACS, 2020,3(5):4356-4366.
[25] SHAO Y J, ZHONG G M, LU Y X, et al. A Nuevo electrolito compuesto de vitrocerámica basado en NASICON con iones de Na mejorados. conductividad. Materiales de almacenamiento de energía, 2019,23:514-521.
[26] LENG H Y, NIE J Y, LUO J. Combinando sinterización en frío y sinterización en fase líquida activada por Bi2O3 para fabricar NASICON dopado con Mg de alta conductividad a temperaturas reducidas. Diario de Materiomica, 2019,5(2):237-246.
[27] OH J A S, HE L C, PLEWA A, et al. Electrolito de estado sólido compuesto NASICON (Na3Zr2Si2PO12) con Na+ mejorado Conductividad iónica: efecto de la sinterización en fase líquida. Materiales aplicados ACS & Interfaces, 2019,11(43):40125-40133.
[28] DA SILVA J G P, BRAM M, LAPTEV A M, et Alabama. Sinterización de un electrolito NASICON a base de sodio: un estudio comparativo entre los métodos de sinterización en frío, asistidos en campo y convencionales. Diario de la Sociedad Europea de Cerámica, 2019,39(8):2697-2702.
[29] WANG H, OKUBO K, INADA M, et al. Bajo Cerámica a base de NASICON densificada por temperatura promovida por vidrio Na2O-Nb2O5-P2O5 Sinterización por plasma aditivo y por chispa. Iónicos de estado sólido, 2018, 322:54-60.
[30] HUO H Y, GAO J, ZHAO N, et al. A Escudo interfacial flexible de bloqueo de electrones para litio sólido libre de dendritas baterías metálicas. Comunicaciones de la naturaleza, 2021,12(1):176.
[31] JIA M Y, ZHAO N, HUO HY, et al. Investigación exhaustiva sobre electrolitos de granate hacia Baterías de litio sólidas orientadas a aplicaciones. Reseñas de energía electroquímica, 2020,3(4):656-689.
[32] ZHAO N, KHOKHAR W, BIZ J, et al. Pilas de granate macizo. Julio, 2019,3(5):1190-1199.
[33] VERTRUYEN B, ESHRAGHI N, PIFFET C, et al Alabama. Secado por pulverización de materiales de electrodos para baterías de iones de litio y sodio. Materiales, 2018,11(7):1076.
[34] KOU Z Y, MIAO C, WANG Z Y, et al. Nuevo sólido estructural tipo NASICON Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 Electrolitos con conductividad iónica mejorada para baterías de iones de litio. Sólido Iónicos estatales, 2019,343:115090.
[35] SHEN L, YANG J, LIU G Z, et al. Alto Conductividad iónica y electrolito sólido NASICON resistente a las dendritas para Baterías de sodio totalmente sólidas. Materiales Hoy Energía, 2021,20:100691.
[36] LI Y Q, WANG Z, LI CL, et al. Densificación y mejora de la conducción iónica del sólido de granate de litio. electrolitos mediante sinterización con oxígeno fluido. Revista de fuentes de energía, 2014,248:642-646.



