Categorías
nuevo blog
- Guía de selección de electrolitos para baterías: lo que los gerentes de compras deben saber.
- Equipamiento para laboratorios de pilas de botón: La lista de verificación completa para laboratorios de I+D de baterías
- Comparación de materiales para cátodos de baterías: NMC vs LFP vs NCA
- Tendencias en la fabricación de baterías de iones de litio para 2026: Guía para compradores B2B
- Guía paso a paso del proceso de fabricación de baterías de iones de litio
Etiquetas
Material de cátodo dopado Sb O3 tipo Na0.9Ni0.5Mn0.3Ti0.2O2 para batería de iones de Na
Material del cátodo Sb dopado O3 tipo Na0.9Ni0.5Mn0.3Ti0.2O2 para batería de iones de Na
KONG Guoqiang, LENG Mingzhe, ZHOU Zhanrong, XIA Chi, SHEN Xiaofang. Cátodo Sb O3 dopado tipo Na0.9Ni0.5Mn0.3Ti0.2O2 Material para batería de iones de Na[J]. Revista de materiales inorgánicos, 2023, 38 (6): 656-662.
Resumen
Estabilidad del ciclo y capacidad específica de Los materiales catódicos para baterías de iones de sodio juegan un papel importante en el logro. su amplia aplicación. A partir de la estrategia de introducir medidas específicas heteroelementos para optimizar la estabilidad estructural y la capacidad específica de materiales del cátodo, O3-Na0.9Ni0.5-xMn0.3Ti0.2SbxO2 (NMTSbx, x=0, 0.02, 0.04, 0,06) se preparó mediante un método de reacción simple en estado sólido, y los efectos de Sb cantidad de dopaje sobre las propiedades de almacenamiento de sodio de Na0.9Ni0.5Mn0.3Ti0.2O2 Se investigaron los materiales del cátodo. Los resultados de la caracterización muestran que la Fuerza de repulsión electrostática entre átomos de oxígeno en el metal de transición. La capa se reduce después del dopaje con Sb, mientras que el espacio de la red se expande, lo que favorece la desintercalación de Na+. Mientras tanto, el electrón fuerte la deslocalización causada por el dopaje Sb disminuye la energía de todo el sistema, lo que lleva a una estructura estable, más propicia para la carga cíclica y descarga. La prueba electroquímica muestra que la descarga inicial específica La capacidad del NMTSb0 sin dopar es 122,8 mAh·gâ1 a 1C (240 mA·gâ1), y la tasa de retención de capacidad es sólo del 41,5% después de 200 ciclos. Pero la capacidad específica de descarga inicial de NMTSb0.04 dopado es 135,2 mAh·gâ1 a 1C, y la tasa de retención de capacidad es de hasta el 70% después de 200 ciclos. Este estudio muestra que el cátodo Na0.9Ni0.5Mn0.3Ti0.2O2 tipo O3 dopado con Sb El material puede mejorar significativamente la capacidad específica de descarga inicial y Tasa de retención de capacidad de las baterías de iones de sodio. Nuestros resultados sugieren que Sb La estrategia de dopaje podría ser un enfoque útil para la preparación de altos niveles estables. baterías de iones de sodio.
Palabras claveï¼ Sb dopaje; tipo O3; material catódico; método en fase sólida; amplio voltaje; Na-ion fabricación de baterías
Desde la comercialización de iones de litio Baterías, han sido ampliamente utilizadas en dispositivos electrónicos portátiles, eléctricos. vehículos y almacenamiento de energía electroquímica, etc. Sin embargo, el limitado recursos y la distribución desigual del litio es un factor importante que restringe el desarrollo de baterías de iones de litio. Al mismo tiempo, las reservas de sodio son abundante y ampliamente distribuida, y lo que es más importante, debido a la similitud de las propiedades químicas del litio y el sodio, el principio de funcionamiento de Las baterías de iones de sodio son similares a las de las baterías de iones de litio. Por lo tanto, el Aplicación de baterías de iones de sodio en el campo del almacenamiento de energía a gran escala. ha recibido gran atención.
Materiales catódicos para baterías de iones de sodio.
incluyen principalmente óxidos en capas de metales de transición, compuestos polianiónicos y
Análogos del azul de Prusia. Entre ellos, el óxido en capas NaxTMO2 (TM se refiere a
metal de transición, 0
Entre los diversos materiales NaxTMO2 tipo O3 que se han informado, NaxTMO2 que contiene Ni y Mn ha atraído mucho atención debido a sus abundantes recursos de Ni/Mn y su alta capacidad de almacenamiento. Por ejemplo, el NaNi0.5Mn0.5O2 de tipo O3 tiene una alta capacidad reversible (133 mAh gâ1). Buen rendimiento (30C, 40mAh gâ1) y ciclo de vida largo (70% de retención de capacidad específica después de 500 ciclos a 3,75 C). Sin embargo, todavía existen algunos problemas que restringen aún más su desarrollo, como rendimiento de tasa insatisfactorio, transición de fase compleja durante la carga y descarga, y una rápida caída de la capacidad, especialmente a altas voltajes de 4,1 a 4,5 V. Estudios recientes han demostrado que el dopaje parcial de otros Los elementos pueden mejorar eficazmente la reversibilidad de la transición de fase. Para Por ejemplo, Na0.9Ni0.4Mn0.4Ti0.2O2 dopado con Ti tiene una fase O3-P3 más reversible. transición entre 2,5 y 4,2 V, mayor capacidad específica (197 mAh g-1) y rendimiento del ciclo más estable. NaFe0.2Mn0.4Ni0.4O2 dopado con Fe tiene un alto capacidad reversible (165 mAh g-1) y una transición de fase estable (87% de capacidad retención después de 200 ciclos) en el rango de 4,0-4,3 V.
Además, el dopaje Sb5+ también puede mejorar la estabilidad del ciclo y el voltaje de trabajo de los materiales catódicos. Con el fin de obtener una estructura de material más estable y un rendimiento de velocidad superior en un rango de voltaje más amplio para óxidos en capas de tipo O3. En este estudio, Sb5+ fue parcialmente sustituido por Ni2+ en Na0.9Ni0.5Mn0.3Ti0.2O2 (NMT) por un simple Método de estado sólido para estudiar el efecto del dopaje con Sb en el sistema electroquímico. Rendimiento de óxidos en capas y cambio de reversibilidad de la fase O3-P3. transición en un amplio rango de voltaje.
1 Método experimental
1.1 Preparación del material
Na0.9Ni0.5-xMn0.3Ti0.2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06) se prepararon materiales mediante el método de fase sólida. el especifico Los pasos son los siguientes: mezcle Na2CO3, NiO, Sb2O5, MnO2 y TiO2 en el relación estequiométrica correspondiente y añadir una fracción molar adicional del 5% de Na2CO3 teniendo en cuenta la volatilidad del Na a alta temperatura. muélelo uniformemente con un mortero de ágata y con una comprimidora formar un disco fino de Ï16 mm. Tratamiento térmico a 950 °C en atmósfera de aire dos veces, cada vez. durante 12 h. Se utilizó el mismo procedimiento para preparar NMTSb0 sin Sb2O5 de partida. material, y todas las muestras se almacenaron en una caja de guantes para uso futuro.
1.2 Conjunto de batería
El material activo NMTSbx, negro de acetileno. y fluoruro de polivinilideno (PVDF) se pesaron en una proporción de masa de 7:2:1, y Se añadió una cantidad apropiada de N-metilpirrolidona (NMP) para moler y obtener una suspensión mezclada uniformemente. La lechada se recubrió sobre la superficie de aluminio. lámina, y la carga superficial del material activo en el electrodo fue de aproximadamente 2,5 mg cm-2. Se secó al vacío a 80 ° C durante 12 h y luego se cortó en pequeños discos de Ï 12 mm con un microtomo como electrodo positivo. botón CR2032 Las células se ensamblaron en una caja de guantes llena de gas Ar (las fracciones de volumen de el agua y el oxígeno fueron ambos inferiores a 1Ã10-6). Entre ellos, el contraelectrodo. es lámina de sodio metálico, el separador es fibra de vidrio y el electrolito es 1 mol L-1 NaClO4 carbonato de dibutilo + solución de carbonato de fluoroetileno (volumen relación 1: 1).
1.3 Caracterización y ensayo de materiales
El espectro de difracción de rayos X (DRX) de la La muestra se probó utilizando MiniFlex 600 (Rigaku, Japón, Cu Kα) y el cristal La estructura fue refinada aún más por Rietveld a través del análisis estructural. sistema (GSAS + EXPGUI). La morfología microscópica y el tamaño de partícula del Las muestras se observaron mediante un microscopio electrónico de barrido JSM-7610F (JEOL, Japón). (SEM) y microscopio electrónico de transmisión de alta resolución JEOL JEM-2100F (HRTEM). La espectroscopia fotoelectrónica de rayos X (XPS) del estado de valencia del Los elementos se probaron en un espectrómetro Escalab250xi utilizando rayos X acromáticos AlKα. fuente. La relación molar de cada elemento de la muestra se analizó mediante espectrómetro de emisión óptica de plasma acoplado inductivamente (ICP-AES, iCAP 6300). Las mediciones de carga y descarga se realizaron a temperatura ambiente utilizando un Sistema de prueba de baterías Land CT2001A entre 2,0 y 4,2 V, y el electroquímico La espectroscopia de impedancia (EIS) de los electrodos se midió utilizando un CHI660E. estación de trabajo electroquímica (CH Instruments).
2 Resultados y discusión
2.1 Características estructurales de NMTSbx
La composición elemental de todas las muestras. fue determinado por ICP-AES, y los resultados se muestran en la Tabla S1. dentro del rango de error de medición, el contenido real de cada ion metálico es básicamente consistente con la composición del diseño. En el espectro XRD de la Fig. 1 (a), todos las muestras tienen una estructura hexagonal de α-NaFeO2 de tipo O3 (grupo espacial R-3m), consistente con NaNi0.5Mn0.5O2 (JCPDS 54-0887). Se demuestra que el La introducción de Sb en la red NMT no cambia la estructura intrínseca. del material. El proceso de preparación de cátodos de óxido con alto contenido de níquel mediante El método de estado sólido inevitablemente producirá una pequeña cantidad de residuos. componentes inactivos de NiO, y la literatura muestra que el impacto de las trazas La cantidad de NiO en el rendimiento de la batería es insignificante. En la figura 1(b), el Los picos de difracción de NMTSb0.02, NMTSb0.04 y NMTSb0.06 cambiaron a grandes ángulos y picos diversos comenzaron a aparecer en NMTSb0.06. Según el Ecuación de Bragg (nλ=2dsinθ), el tamaño de grano promedio del polvo es cualitativamente analizado. donde n es el orden de difracción, d es el espesor promedio (nm) de los granos de la muestra perpendiculares a la dirección del cristal plano, θ es el ángulo de difracción correspondiente a la difracción más fuerte pico, y λ es la longitud de onda de los rayos X (nm). Los resultados del cálculo del plano cristalino. muestran que el tamaño de grano de la muestra disminuye después del dopaje con Sb, que es relacionado con la diferencia en el radio iónico de Sb (0,06 nm) y Ni (0,069 Nuevo Méjico). Según el teorema de Vegard, esto también significa que una solución sólida La reacción ocurrió durante la formación de NMTSbx.
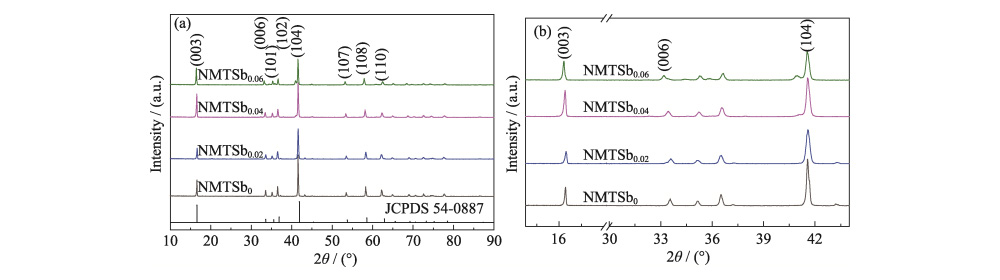
Fig. 1 Encuesta (a) y patrones XRD ampliados (b) de NMTSbx (x=0, 0,02, 0,04, 0,06)
La Figura 2 (a, b) muestra el XRD refinado Patrones de Rietveld de NMTSb0 y NMTSb0.04, y los parámetros de red detallados se muestran en la Tabla S2. Se puede ver que los parámetros de red de NMTSb0.04 (a=b=0,29790 nm) se reducen ligeramente en comparación con el NMTSb0 original (a=b=0,29812nm). Esto también se atribuye al hecho de que el radio iónico de Sb (0,06 nm) es más pequeño que el de Ni (0,069 nm), lo que concuerda con la Análisis XRD. La c (c = 1,608391 nm) de NMTSb0,04 aumentó en comparación con el de NMTSb0 (c=1,600487 nm). La razón principal es que el parámetro de red a/b es sensible al cambio de la longitud del enlace (Ni/Mn/Ti/Sb)-O del plano basal de la estructura en capas, y la incorporación de Sb acorta el enlace longitud. Esto provoca la repulsión electrostática entre los átomos de oxígeno en el capa continua de metal de transición (Ni/Mn/Ti/Sb) se haga más grande, lo que lleva a una aumento en c. Además, después del cálculo, la c/a de NMTSb0 y NMTSb0.04 no no cambiaron mucho, fueron 5,36 y 5,39 respectivamente, ambos fueron mayores que 4,99, lo que indica que las muestras dopadas mantuvieron una buena estructura en capas.
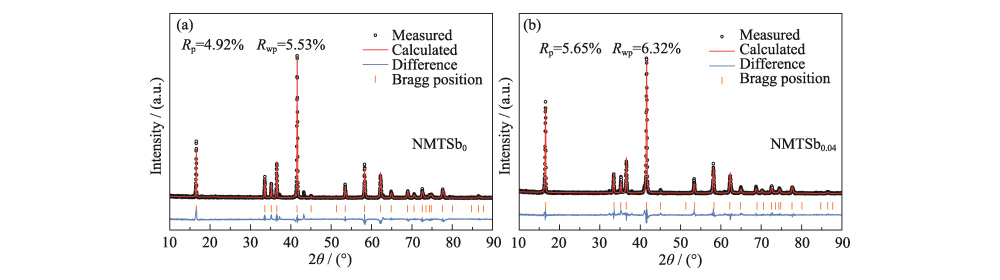
Fig. 2 Rietveld Patrones XRD de refinamiento de NMTSb0 (a) y NMTSb0.04(b)
La Figura 3 muestra las imágenes SEM de NMTSb0 y NMTSb0,04. Ambos productos están compuestos por una gran cantidad de micronanoescala. Discos finos con espesor uniforme y bordes claros. Especialmente después del dopaje Sb, la superficie de las escamas es más suave y no faltan las escamas hexagonales. Estructura con bordes y esquinas cortantes. Análisis elemental EDS de área seleccionada de NMTSb0.04 muestra que los elementos Na, O, Ni, Ti, Mn y Sb están distribuidos uniformemente en la muestra, lo que también demuestra que los elementos Sb se han dopado con éxito en la estructura intrínseca de NMTSb0.

Fig. 3 SEM imágenes y mapeos EDS de NMTSb0 (a, b) y NMTSb0.04 (c, d)
Las microestructuras de NMTSb0 y NMTSb0.04. HRTEM observó más a fondo y los resultados se muestran en la Figura S1. En Figura S1 (a, c), las partículas antes y después del dopaje Sb están conectadas o superpuestos y macroscópicamente aparecen como una hoja o aproximadamente Estructura circular o poligonal. Las imágenes HRTEM de la Figura S1 (b, d) muestran la franjas de red del material, y los espacios de red de NMTSb0 y NMTSb0.04 son 0,238 y 0,237 nm, respectivamente. Ambos corresponden al (101) plano cristalino, y el efecto del dopaje Sb en el espaciado de la red es consistente con los resultados del análisis XRD. Los recuadros de la Figura S1 (b, d) son los puntos de el patrón de difracción de electrones del área seleccionada (SEAD) de NMTSb0 y NMTSb0.04, lo que demuestra que los NMTSb0 y NMTSb0.04 obtenidos tienen buena cristalinidad.
La espectroscopia de fotoelectrones de rayos X (XPS) de la Figura S2 muestra los resultados del estado de oxidación de los elementos Mn, Ni, Ti y Sb. en NMTSb0 y NMTSb0.04. En la Figura S2 (a), los dos picos principales de NMTSb0 en 877 y 850 eV corresponden a Ni2p1/2 y Ni2p3/2, respectivamente, y ambos pertenecen a Ni2+ en la muestra. El pico de energía de enlace a 858,2 eV es un satélite común pico en el elemento Ni. El Ni2p1/2 de NMTSb0.04 se divide en dos picos, lo que indica que la introducción de Sb en la red NMTSb0 puede reducir el número de electrones externos alrededor del Ni, lo que resulta en una fuerte deslocalización de electrones efecto. Los metales de transición tienen orbitales d más deslocalizados, lo que puede mejorar la interacción metal-metal de los octaedros que comparten lados MO6 en las capas estructura, inhibiendo así el colapso de los octaedros MO6 y aliviando las reacciones secundarias del oxígeno reticular y del electrolito. durante el proceso de carga-descarga, la estructura del material de óxido en capas se vuelve más estable, lo que indica que una fuerte deslocalización de electrones es beneficiosa para la estabilidad estructural de NMTSb0.04. Para el elemento Mn, el pico Mn2p3/2 en 642 eV y el pico Mn2p1/2 a 652 eV en la Figura S2 (b) indican la presencia de Mn en el estado de valencia +4 tanto en NMTSb0 como en NMTSb0.04. El pico Mn2p3/2 en 643eV se puede combinar con el pico Mn3+. La configuración octaédrica de Mn3+ se deformará, lo cual es causado por la distorsión de Ginger-Taylor. la disolucion del elemento Mn provocará una rápida disminución de la capacidad, mientras que el Ti en NMTSb0,04 reemplaza parte de Mn, y la reducción del contenido de Mn también puede estabilizar el marco estructural del material, inhibiendo así la rápida disminución de capacidad de la batería causada por el efecto jengibre-Taylor. La energía de enlace típica. picos de Ti2p1/2 y Ti2p3/2 a 457,3 y 453,1 eV para NMTSb0 en la Figura S2 (c) corresponden al estado de valencia estable +4 del Ti. Mientras que Ti2p1/2 y Ti2p3/2 los picos en 454,1 y 463,9 eV de NMTSb0.04 corresponden a Ti en la valencia +3 estado. Desde la perspectiva de la compensación de cargos, esto se debe principalmente a la Reacción de reducción de Ti después de la introducción de Sb5+ de alta valencia. Durante Después de la reacción de carga-descarga, el Ti4+ continuó existiendo en forma estable, lo que se verificó en la curva de voltamperometría cíclica (CV) de NMTSb0.04, como se muestra en Figura 4. Esto también muestra que la fuente de capacidad de la batería no tiene nada que ver con el par redox Ti4+/Ti3+. Además, los picos de energía de enlace de NMTSb0.04 a 529â536 eV en la Figura S2 (d) confirma la presencia de Sb.
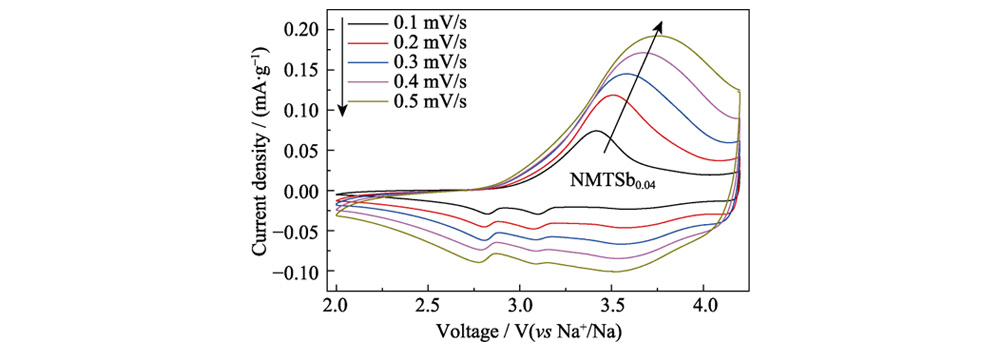
Fig. 4 CV curvas de NMTSb0.04 material del cátodo
2.2 Rendimiento electroquímico
La figura 5 muestra la electroquímica. Gráfico de impedancia de Nyquist de NMTSbx. Entre ellos, el semicírculo en el medio y La región de alta frecuencia representa la resistencia de transferencia de carga (Rct) entre El electrolito y el electrodo, y la línea oblicua en la baja frecuencia. La región representa la resistencia de Warburg causada por la difusión de sodio. iones. Al montar el circuito equivalente se muestra que el Rct de NMTSb0 y NMTSb0.04 son 1185,4 y 761 Ω, respectivamente. A medida que aumenta el contenido de dopaje Sb, el La impedancia de la muestra también disminuye. Cuando x=0,04, la impedancia del muestra alcanza el valor mínimo. Aumentar aún más el contenido de dopaje Sb conduce a un aumento de la impedancia. Cuando x = 0,06, la impedancia excede la de la muestra NMTSb0. Un contenido de dopaje adecuado puede obtener el metal óptimo. El espaciado entre capas de la estructura en capas garantiza un transporte suave de electrones. Canales, ayudan a mejorar las características dinámicas de NMTSb0.04, y al mismo tiempo Al mismo tiempo, tenga en cuenta la estabilidad de la estructura general.
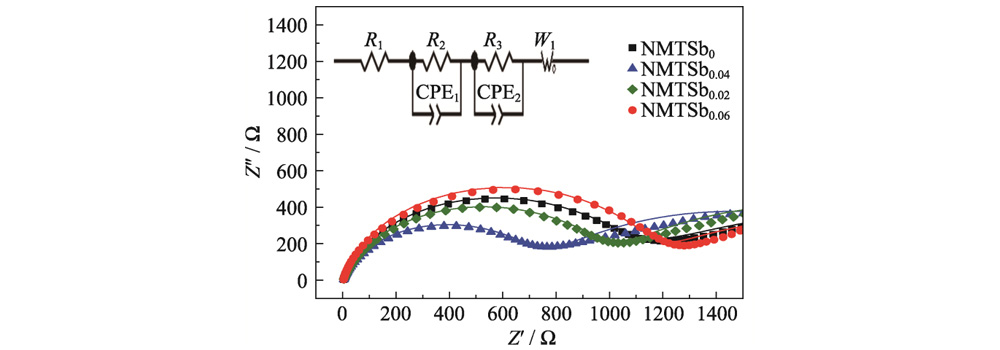
Fig. 5 Electroquímica espectros de impedancia de NMTSbx
Bajo la condición de densidad de corriente de 1C (240 mA·gâ1) y rango de voltaje de 2,0-4,2 V, el sodio rendimiento de almacenamiento de la batería de iones de Na con NMTSbx como electrodo probado. Como se muestra en la Figura 6 (a), las capacidades reversibles de NMTSbx (x = 0, 0,02, 0,04, 0,06) las muestras son 122,8, 128,0, 135,2 y 103,9 mAh gâ1, respectivamente. La diferencia en la capacidad específica se debe a contenido de dopaje diferente. La estrategia de sustitución de elementos químicos puede suprimir la transición de fase irreversible y mejorar el transporte de iones de sodio cinética. Las ventajas se resumen a continuación: reemplazan los altamente activos elementos con elementos electroquímicamente inactivos y estructuralmente estables, tales como como prevenir la mezcla de cationes aumentando la barrera energética de la migración de Ni2+, y reducir el oxígeno liberado durante el ciclo electroquímico mediante Fortalecimiento de los enlaces metal-oxígeno. Dopaje o sustitución de sitios de metales de transición Puede inhibir significativamente la transición de fase, inhibir el ion del metal de transición. migración, y mejorar la estabilidad química y electroquímica de Materiales desodiumizados. Se debe explorar el contenido específico del dopaje. según el tipo de elemento dopante y la estructura intrínseca. . en el Por un lado, el dopaje con iones metálicos de alta valencia puede mejorar la conductividad masiva. del material después de que los iones metálicos ingresan al interior de la red. Cuando la fracción molar de dopaje es superior al 1% (relación estequiométrica x0.01), la resistividad disminuirá rápidamente, lo que tendrá un gran influencia sobre la conductividad. Por otra parte, una cantidad demasiado elevada de dopaje inevitablemente reduce el contenido de pares redox en el sistema y afecta la densidad de energía del sistema, mientras que una cantidad muy pequeña de dopaje no será suficiente para estabilizar la estructura de materiales de óxido en capas. En este estudio, NMTSbx(x=0, 0,02, 0,04, 0,06), x es la relación estequiométrica y el valor real El contenido de dopaje es 2%, 4% y 6% por fracción molar, respectivamente.
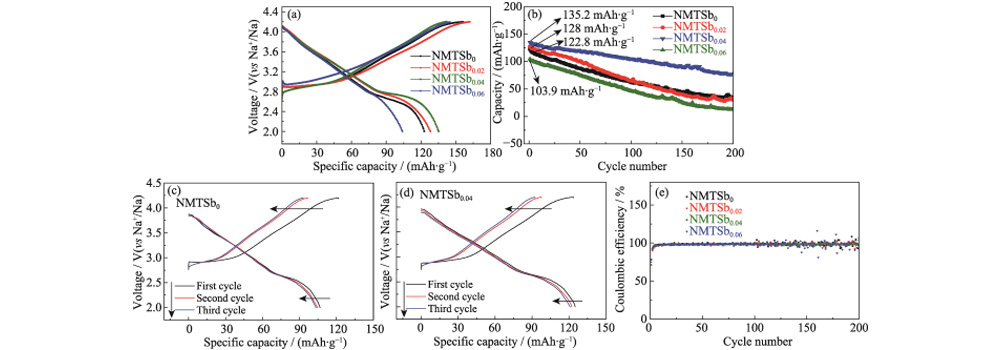
Fig. 6 Rendimiento de baterías de iones de Na con NMTSbx como electrodos
(a) Carga y curvas de descarga de baterías de iones de Na con muestras como electrodos para la primera ciclo a 1C; (b) Rendimiento cíclico de baterías de iones de Na con muestras como electrodos a 1C durante 200 ciclos; (c, d) Carga y descarga curvas de baterías de iones de Na con muestras como electrodos para los 3 ciclos iniciales a 5C; (e) Eficiencias culombicas de baterías de iones de Na con NMTSbx como electrodos para 200 ciclos a 1C Figuras coloridas disponibles en sitio web
En la Fig. 6 (a), la curva de carga-descarga de la muestra no dopada NMTSb0 obviamente contiene múltiples mesetas de voltaje y pasos, lo que indica que múltiples transiciones de fase de hexagonal a monoclínica puede ocurrir en la estructura en capas. Sin embargo, si bien el deslizamiento entre capas del Cuando se produce una capa de metal de transición, la curva general de carga-descarga es relativamente liso. Las tres plataformas de voltaje por encima de 3,00 V tienden a verse borrosas. Para NMTSb0, la curva de carga se divide principalmente en dos partes: la sección de pendiente alrededor de 3,00-3,80 V y la sección de meseta larga por encima de 3,80 V. Sin embargo, cuando Sb se introdujo, el voltaje inicial del segmento de la plataforma aumentó por encima 4,00 V. Para la curva de descarga, la meseta larga suele producirse en la tensión rango de 2,50 a 2,75 V. La apariencia de la meseta de voltaje se puede atribuir a la transformación de la fase O3 en la fase P3, mientras que la pendiente segmento cuando el voltaje aumenta es causado por la reacción de la solución sólida con la estructura P3. La Figura 6(b) es una comparación del rendimiento del ciclo de Electrodos NMTSbx (x = 0, 0,02, 0,04, 0,06) a una densidad de corriente de 1C. Es Vale la pena señalar que la estabilidad cíclica del material del cátodo NMTSb0.04 es la mejor, y alrededor del 70% de la capacidad reversible se puede retener después de 200 ciclos. Por el contrario, la capacidad específica del electrodo NMTSb0 decae muy rápidamente, con un valor inicial de 122,8 mAh g-1, que baja a 51 mAh g-1 después de 200 ciclos, y sólo queda el 41,5% de la capacidad específica. En la figura 6(c, d), incluso a una velocidad muy alta de 5C (1200 mA gâ1), el La retención de capacidad específica del electrodo NMTSb0.04 sigue siendo del 92,6% (125,3 mAh gâ1). La capacidad específica del NMTSb0 electrodo es sólo 106,7 mAh·gâ1, que es superior a otros óxidos en capas de tipo O3 reportados. La capacidad específica de descarga inicial. de O3-Na(Ni1/3Mn1/3Fe1/3)0.95Al0.05O2 preparado por el grupo de Yan a razón de 0.1C es 145,4 mAh·gâ1. Y después de 80 ciclos a una velocidad de 0,2 °C, el específico reversible La capacidad es de 128,4 mAh·gâ1. El O3-NaNi0.5Mn0.5O2 preparado por el grupo de investigación de Guo tiene una capacidad específica de 80 mAh·g-1 en el rango de voltaje de 2-4 V a una velocidad de 2C. La Figura 6 (e) presenta la eficiencia de Coulombic del Batería de iones de Na durante ciclos continuos a 1C. Entre ellos, el Coulombiano. La distribución de eficiencia del electrodo NMTSb0.04 es estable y tiende a una línea recta, manteniéndose básicamente en 98%, lo que también indica que su La estructura en capas es más estable. Sin embargo, la eficiencia de Coulombic del El electrodo NMTSb0 fluctuó significativamente después de 140 ciclos, y hubo una gran salto cuando estaba cerca de los 200 ciclos. La batería ensamblada con NMTSb0.04 después de 200 ciclos fue desmontado y procesado, y el espectro XRD Se probó la lámina del electrodo, los resultados se muestran en la Figura S3. El XRD Los picos de difracción de la pieza polar NMTSb0.04 no cambiaron significativamente después ciclado, lo que indica que el cambio de fase irreversible del cátodo NMTSb0.04 El material fue suprimido después del dopaje.
3 Conclusión
En este estudio, Na0.9Ni0.5-xMn0.3Ti0.2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06), un material de cátodo de óxido en capas para baterías de iones de sodio, se preparó mediante un método conveniente de estado sólido. Es Las partículas están compuestas de escamas de micronanoescala con espesor uniforme y bordes claros y el tamaño del grano disminuye después de que el Sb reemplaza parte del Ni. Al Al mismo tiempo, el dopaje de Sb provoca una fuerte deslocalización de electrones, que reduce la energía de todo el sistema y obtiene una estructura estable que es más propicio para ciclos de carga y descarga a largo plazo. en la electroquímica prueba en el rango de 2,00-4,20 V, el dopaje de Sb suprimió la fase irreversible transición del material del cátodo y mejoró la plataforma de voltaje de trabajo. Cuando se carga y descarga a una velocidad de 1C, la capacidad específica de descarga inicial de NMTSb0.04 es 135,2 mAh·g-1, y la tasa de retención de capacidad después de 200 ciclos es 70%. La retención de capacidad específica puede alcanzar el 92,6% (125,3 mAh·gâ1) a una velocidad de 5C.
Información complementaria

Fig. S1 HRTEM imágenes de NMT (a, b) y NMTSb0.04 (c, d) con recuadro en (b, d) que muestra las imágenes SEAD correspondientes
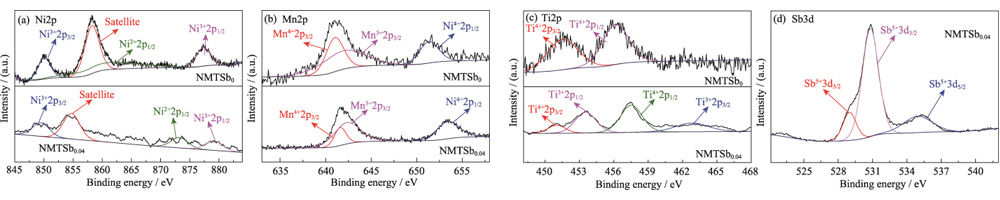
Fig. S2 (a) Espectros XPS de Ni2p, (b) Mn2p, (c) Ti2p y (d) Sb3d de NMTSb0 y NMTSb0.04
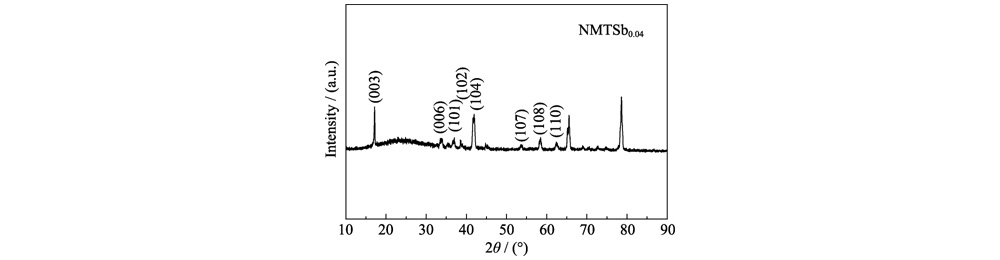
Fig. S3 DRX patrón de NMTSb0.04 como material catódico de Batería de iones de Na después de 200 ciclos
Tabla S1 Resultados de ICP-AES de O3-NMTSbx (x=0, 0,02, 0,04, 0,06) (relación estequiométrica)
|
Na |
Ni |
Mn |
Ti |
Sb |
|
|
NMTSb0 |
0,913 |
0,486 |
0,288 |
0,181 |
0 |
|
NMTSb0.02 |
0,924 |
0,471 |
0,284 |
0,186 |
0,023 |
|
NMTSb0.04 |
0,920 |
0,452 |
0,287 |
0,184 |
0,039 |
|
NMTSb0.06 |
0,929 |
0,435 |
0,279 |
0,184 |
0,061 |
Tabla S2 Parámetros de red de materiales con NMTSb0 y NMTSb0.04
|
a/nm |
b/nm |
c/nm |
V/nm3 |
Rwp/% |
RP/% |
|
|
NMTSb0 |
0,29812 |
0,29812 |
1.600487 |
0,1232 |
4,92 |
5.53 |
|
NMTSb0.04 |
0,29790 |
0,29790 |
1.608391 |
0,1236 |
5.65 |
6.32 |



